ICON公司发布了《脑外伤:从鉴定生物标志物到提高临床试验效率》。
报告指出,临床研究行业一直在讨�������论确保临床试验质量的方法的彻底转变,其中涉及针对现场监测和数据处理基于风险的方法的针对性更强。这一转变的主要目标是提高����临床试验研究的效率,有效性和质量,并提高患者的安全性并生成数据。
监管机构认识到,在全球跨国研究的时代,传统的临床试验监测方法已不再可持续。美国食品药品监督管理局(FDA)和欧洲药品管理局(EMA)均于20������13年发布了基于风险的监测指南,国际协调会议(ICH)指南Q9
中概述了质量风险管理原则。 FDA和EMA指南的目的是通过对研究行为�������和报告的最重要方面进行监督来提高临床试验中患者的安全性和数据质量。
一、ICON方法
RBQM旨在预防,检测,减轻和学习临床试验中的风险和错误,同时保持符合法规指导的检查准备。
图1 RBOM框架
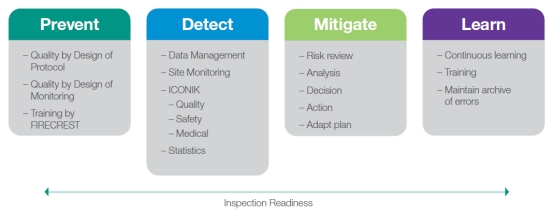
在RBQM框架内,初始风险评估分������类建议一种最佳的监测策略,而先发的临床试验风险则决定是否部署ICONIK集中式监测和分析。
ICONIK是功能强大的集成整合,标准化和可视化来自多个来源的运营和临床数据的信息平台,可提供所有研究信息的整体�������视图。
二、避免
在可能的情况下,应考虑研究者和患者的观点������,以便改进协议并在实现对研究过程的依从性方面最大程度地支持研究站点。
有效预防和获得高质量数据的下一步是有效的员工培训。
在RBQM框架内,FIRECREST培训解决方案提供定制的,基于研究的,基于Web的培训模块,以向现场人员和研究团队提供培训。 ������
由研究人员领导的开发������团队生成了动态且引人入胜的培训解决方案,以促进对现场人员和研究团队的培训。
三、探测
RBQM通过将中央和现场监视整合到最������佳技术,人员和过程范式中,从而能够设计出一种有效的检测方法,以实现��������质量,完整性,安全性以及性能风险和错误。
集中监控集中在集中的可视化数据或单个集合中的集中可用数据。
四、缓解
检测到的错误,其根本原因分析和缓解措施已记录在临床试验管理系统(CTMS)�����中。
按照商定的频率,举行整体质量和风险审查会议(QRRM),以验证所选监视策略的有效性和效率。
������QRRM的目的是审查和保持对研究过程中发现和缓解的研究紧急风险和问题的监������督。
跨职能项目团队的项目监督可能导致风险重新评估,监控策略,数据的适应性,审查计划和/或分配给站点,国家或整体研究的资源。
五、合作学习
根据QRRM的结果,项目团队������可以根据需要向研究团队或整个组织发布“经验教训”项目。 QRRM也可能导致研究或公司�������培训内容的发展或更新。
本文由@云闲 原创发布于三个皮匠报告网站,未经授权禁止转载。
数据来源:《ICON公司:脑外伤:从鉴定生物标志物到提高临床试验效率》。

 sgpjbg002
sgpjbg002 工作日 8:30 - 17:30
工作日 8:30 - 17:30