我国药品注册分类主要分为了�������化学药����品、预防用生物制品、治疗用生物制品、中药四大类别。下面是其子类别及细分类别的详细介绍。
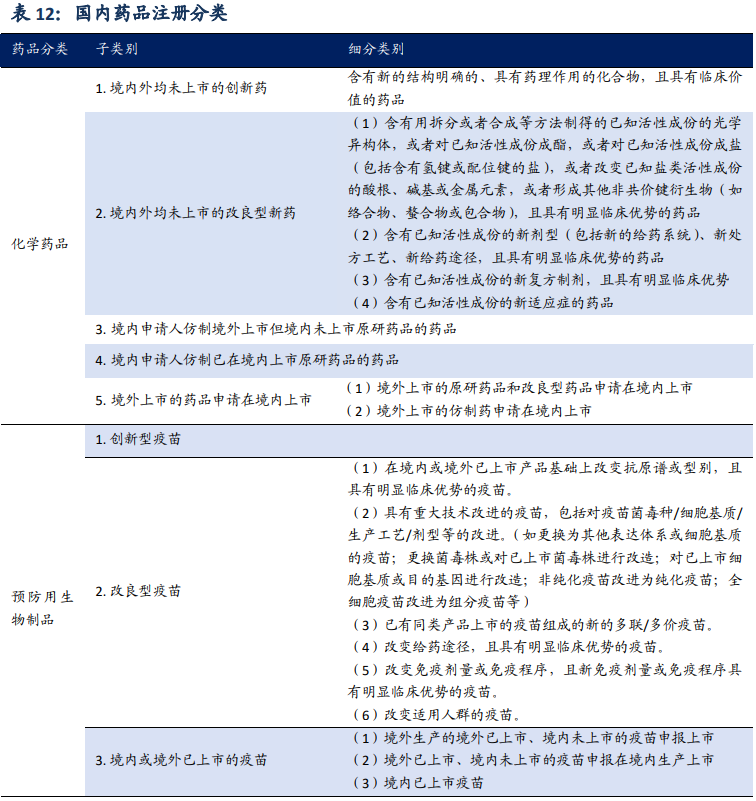
一、化学药品
子类别
【1】境内外均未上市的创新药
细分类别:含有新的结构明确的、具有药理作用的化合物,且具有临床价值的药品。
【2】境内外均未上市的改良型新药
细分类别:(1)含有用拆分或者合成等方法制得的已知活性成份的光学异构体,或者对已知活性成份成酯,或者对已知活性成份成盐(包括含有氢键或配位键的盐),或者改变已知盐类活性成份的酸根、碱基或金属元素,或者形成�����其他非共价键衍生物(如络合物、螯����合物或包合物),且具有明显临床优势的药品(2)含有已知活性成份的新剂型(包括新的给药系统)、新处方工艺、新给药途径,且具有明显临床优势的药品(3)含有已知活性成份的新复方制剂,且具有明显临床优势(4)含有已知活性成份的新适应症的药品。
【3】境内申请人仿制境外上市但境内未上市原研药品的药品
【4】境内申请人仿制已在境内上市原研药品的药品
【5】境外上市的药品申请在境内上市
细分类别:(1)�����境外上市的原研药品和改良型药品申请在境内上市(2)境外上市的仿制药申请在境内上市)。
二、预防用生物制品
子类别
【1】 创新型疫苗
【2】 改良型疫苗
细分类别:(1)在境内或境外已上市产品基础上改变抗原谱或型别,且具有明显临床优势的疫苗(2)具有重大技术改进的疫苗,包括对疫苗菌毒种/细胞基质/�����
生产工艺/剂型等的改进。(如更换为其他表达体系或细胞基质的疫苗;更换菌毒株或对已上市菌毒株进行改造;对已上市细胞基质或目的基因进行改造;非纯化疫苗改进为纯化疫苗;全细胞疫苗改进为组分疫苗等)(3)已有同类产品上市的疫苗组成的新的多联/多价疫苗(4)改变给药途径,且具有明显临床优势的疫苗(5)改变免疫剂量或免疫程序,且新免疫剂量或免疫程序具有明显临�����床优势的疫苗(6)改变适用人群的疫苗。
【3】境内或境外已上市的疫苗
细分类别:(1)境外生产的境外已上市、境内未��上市的疫苗申报上市(2)境外已上市、境内未上市的疫苗申报在境内生产上市(3)境内已上市疫苗。
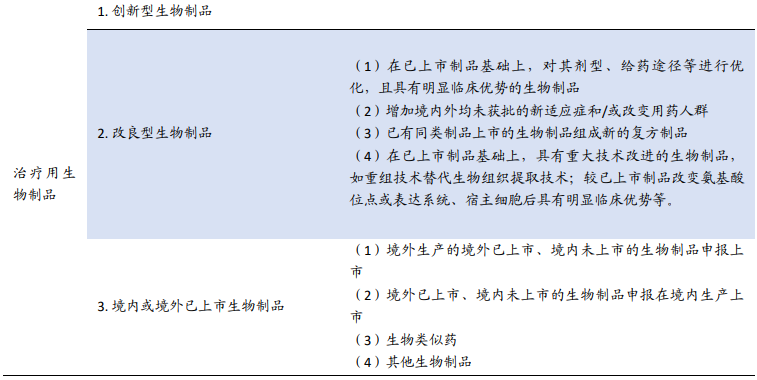
三、治疗用生物制品
子类别
【1】 创新型生物制品
【2】 改良型生物制品
细分类别:(1)在已上市制����品基础上,对其剂型、给药途径等进行优化,且具有明显临床优势的生物制品(2)增加境内外均未获批的新适应症和/或改变用药人群(3)已有同类制品上市的生物制品组成新的复方制�������品(4)在已上市制品基础上,具有重大技术改进的生物制品,如重组技术替代生物组织提取技术;较已上市制品改变氨基酸位点或表达系统、宿主细胞后具有明显临床优势等。
【3】境内或境外已上市生物制品
细分类别:(1)境外生产的境外已上市、境内未上市的生物制品申报上市(2)境外已上�������市、境内未上市的生物制品申报在境内生产上市(3)生物类似药(4)其他生物制品。
四、中药
子类别
【1】中药创新药
细分类别:(1)中药复�����方制剂,系指由多味饮片、提取物等在中医药理论指导下组方而成的制剂。(2)从单一植物、动物、矿物等物质中提取得到的提取物及其制剂。(3)新药材及其制剂,即未被国家药品标准����、药品注册标准以及省、自治区、直辖市药材标准收载的药材及其制剂,以及具有上述标准药材的原动、植物新的药用部位及其制剂。
【2】中药改良型新药
细分类别:(1)改变已上市中药给药途径的制剂,�����即不同给药途径或不同吸收部位之���������间相互改变的制剂。(2)改变已上市中药剂型的制剂,即在给药途径不变的情况下改变剂型的制剂。(3)中药增加功能主治。(4)已上市中药生产工艺或辅料等改变引起药用物质基础或药物吸收、利用明显改变的。
【3】古代经典名方中药复方制剂
细分类别:(1)按古代经典名方目录管理的中药复方制剂。(2)其他来������源于古代经典名方的中药复方制剂。包括未按古代经典名方目录管理的古代经典名方中药复方制剂������和基于古代经典名方加减化裁的中药复方制剂。
【4】同名同方药
以下就是国内药品注册分类的详细介绍了,更多相关内容,敬请关注三个皮匠报告的行业知识栏目了解。
数据来源:CDE, 东吴证券研究所

本文由@-YANYI 发布于三个皮匠报告网站,未经授权禁止转载。
推荐阅读
什么是中药饮片、中成药、中药配方颗粒?三者对比分析
化学制药与生物制药有什么区别?行业分类、发展趋势及龙头股介绍
DTP药房有哪些?中国十大DTP药房排名一览

 sgpjbg002
sgpjbg002 工作日 8:30 - 17:30
工作日 8:30 - 17:30