一、什么是免疫治疗?
细胞免疫治疗是将免疫细胞(多为T细胞)输给患者来治疗血液癌症及实体瘤�����的一种免疫疗法,其中,T细胞通常取自患者自身的血液或肿瘤������组织,在实验室中大量扩增,然后回输给患者以帮助免疫系统杀死肿瘤细胞。
根据产品类型的不同,细胞免疫治疗又可进一步分为活化的自体淋巴细胞(AAL)、CIK、C�����AR-T 等多种类型。
主要细胞免疫治疗方案对比

肿瘤免疫疗法旨在提高肿瘤细胞的免疫原性,消除肿瘤免疫抑制网络来激活并增强机体免疫系统������对于肿瘤细胞的识别、响应、杀伤能力,从而能够通过调控自身免疫机能达到长期且有效的抗肿瘤治疗。
当�������前在肿瘤治疗领域有许多新的免疫治疗方法涌现出来,并在临床应用上取得了一定的成功。肿瘤免疫治疗主要包括以下四种方法:过继性免疫效应细胞疗法、免疫检查点抑制剂、肿瘤免疫疫苗、肿瘤特异性单克隆抗体。
目前,肿瘤免疫疗法开发主要集中在以下几个方面:
(1)以PD-1、CTLA-4为代表的免疫检查点抑制剂
(2)以OX40、41-BB为代表的增强T细胞信号的激活类单抗
(3)以CAR-T、CAR-NK为代表的过继性细胞治疗
(4)以TGF-β为代表的靶向细胞因子药物
(5)溶瘤病毒
(6)以PD-1/CTLA-4、PD-(L)1/TGF-β为代表的双功能抗体、多功能抗体药物
二、全球肿瘤免疫市场规模与发展现状
根据沙利文报告数据,2019年全球肿瘤免疫治疗市场规模已经达290亿美元,2015
年到2019年期间,年复合增长率达������58.6%。预计2024年全球肿瘤免疫治疗市场增长至957亿美元,年复合增长率高达27.0%;2024年至2030年,将继续保持11.4%的年复合增长率,于2030增至1832亿美元。
全球肿瘤免疫治疗市场规模广阔(单位:亿美元)

截止2021年3月,全球共12款PD-1、PD-L1单抗药物获批。据沙利文报告预测,全球PD-1单抗药物市场规�������模迅速扩大,在2015年到2019年期间的年复合增长率高达 96.3%,从2015 年的16亿美元增至2019年的232亿美元市场规模,预计到2024年增长至678亿美元,23.9%的年复合增长率。
全球PD-1 单抗市场仍在爬坡,峰值可达 770 亿美元(单位:亿美元)

三、中国肿瘤细胞免疫治疗的市场规模与发展现状
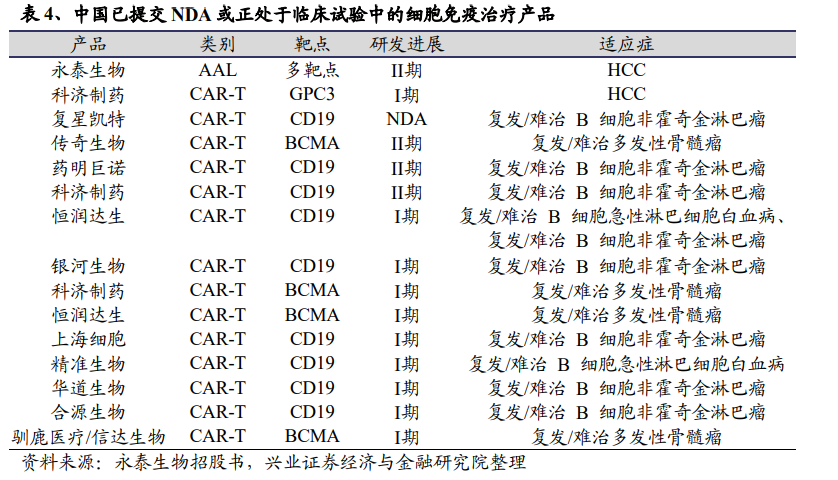
截至 2021年 4 月,我国有�����15 种细胞免疫治疗产品处于临床试验阶段。有13 种产品用于治疗血液癌症,14 款为CAR-T细胞产品,另外一款为 AAL 产品。中国尚未有上市的细胞免疫治疗产品,当前市场参与者将重点����放在开发CAR-T细胞产品上。
中国已提交NDA或正处于临床试验中的细胞免疫治疗产品
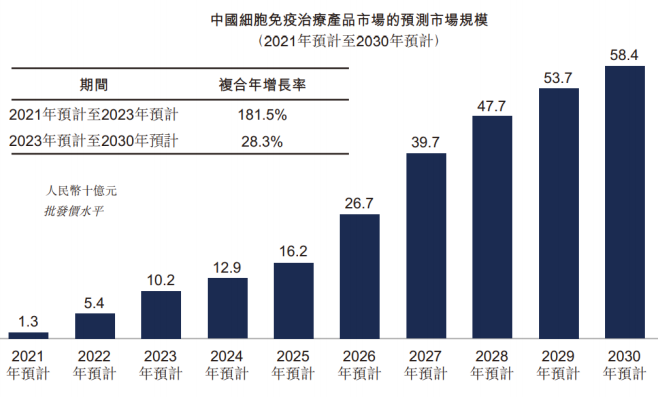
预计2021-20�������23年,中国的细胞免疫治疗产品市场规������模将由13亿上升到102亿元,复合年增长率达181.5%,并且将于2030年达到584亿元,其中2023年至2030年的复合年增长率为28.3%。
2021-2030 年中国细胞免疫治疗产品市场的预测市场规模
四、肿瘤免疫疗法研发进展
1、免疫治疗开创
1796年,Edword Jenner成功开发出首个牛痘疫苗
1890年,癌症免疫疗法之父Dr.Colley为肿瘤患者注射链球菌����(科莱毒素),治疗了上百例肿瘤患者
2、肿瘤免疫生物学解读
1909年,Paul Erich提出设想“肿瘤可以被免疫系统压制”。
1957年,Thomas和Burnet首次提出“肿瘤免疫检查”,揭示淋巴细胞������在������清除异常细胞中起监察作用,发现干扰素。
1959年,揭示膀胱癌荷瘤小鼠上BCG细菌的抗肿瘤作用。
1960-1980年,发现T细胞、树突细胞、NK细胞、IL-2。
1987年,Brunet发现首个免疫检查点CTLA-4。
1991年,首次发现人类肿瘤相关抗原。
1998年,揭示了4-1BB在T细胞发挥抗肿瘤作用中的机制。
肿瘤免疫编辑假说:清除状态、平衡状态、逃逸状态。

3、免疫疗法的应用探索
1975年,在实验室首次成功制备单抗。
1976年,Morales应用BCG治疗膀胱癌。
1986年,研发全球首个重组疫苗,HBV疫苗。
1991年,FDA批准IL-2作为免疫制剂治疗转移性肾癌。
1998年,首个单抗药物利妥昔单抗获FDA批准。
FDA批准IL-2治疗黑色素瘤
2000年,启动伊匹木单抗的首个临床试验。
2010年,FDA批准sipuleucell-T治疗前列腺癌。
4、全球成果加速落地
2011年,FDA批准全球首个免疫检查点抑制剂伊匹木单抗。
2014年,FDA批准全球首个PD-1单抗纳武利尤单抗上市,同期帕博利珠单抗上市。
2015年,FDA批准首个治疗黑色素瘤的溶瘤病毒上市。
2016年,FDA批准全球首个PD-L1单抗阿替利珠单抗上市。
2017-2018年,FDA批准CAR-T疗法治疗AML及其他淋巴瘤。
2018年,“通过抑制免疫抑制网络治疗肿瘤”学说获得诺贝尔奖。
5、国内PD-1商业化兑现
2018年,国内首家PD-1单抗特瑞普利单抗获NMPA批准,治疗经治的黑色素瘤。
2018年,信达生物信迪利单抗获NMPA批准,治疗三线cHL,2019年进入国家医保目录。
2019年,恒瑞医药卡瑞利珠单抗获得NMPA批准。
2019年,百济神州替雷利珠单抗获得NMPA批准。
2020年,国内四家PD-1纳入国家医保目录。
更多行业现状分析,敬请关注三个皮匠报告行业分析栏目。
内容来源:
《君实生物-行稳致远君子务实-210823(49页).pdf》

 sgpjbg002
sgpjbg002 工作日 8:30 - 17:30
工作日 8:30 - 17:30